Search
分子

分子(ぶんし、英: molecule)とは、2つ以上の原子から構成される電荷的に中性な物質を指す。厳密には、分子は少なくとも1つ以上の振動エネルギー準位を持つほどに充分に深いエネルギーポテンシャル表面のくぼみを共有する原子の集まりを指す。この基準を満たすイオンは、文脈によって含まれる場合もあれば含まれない場合もある。量子物理学、有機化学、生化学の分野では、イオンとの区別をせず、多原子イオンを指して分子が使われることが多い。
概要
分子には、酸素分子(酸素原子2つ、O2)のように1つの化学元素の原子からなる等核分子と、水(水素原子2つと酸素原子1つ、H2O)のように2つ以上の元素からなる異核分子がある。気体分子運動論では、あらゆる気体粒子はその組成にかかわらず分子と呼ばれることが多い。これは、希ガスが単原子で安定な化学種であるため(単原子分子とも呼ばれる)、分子が2つ以上の原子を含むという要件を緩和したことによる。水素結合やイオン結合など非共有結合で結合された原子や複合体は、通常、単一分子とはみなされない。
分子のような概念は古くから議論されてきたが、分子とその結合の本質に関する近代的な研究は17世紀に始まった。ロバート・ボイル、アメデオ・アヴォガドロ、ジャン・ペラン、ライナス・ポーリングといった科学者たちによって、時間をかけて洗練された分子の研究は、今日では分子物理学または分子化学として知られている。
語源
メリアム=ウェブスターやオンライン・エティモロジー・ディクショナリーによると、「分子(molecule)」という言葉は、ラテン語の「moles」すなわち「質量の小さな単位」に由来する。語源はフランス語の molécule(1678)で、ラテン語の moles 「mass, barrier(質量、境界)」の指小辞である新ラテン語の molecula に由来する。18世紀後半までラテン語の形でしか使われなかったこの言葉は、デカルトの哲学書で使われたことで人気を博した。
歴史
分子の構造に関する知識が増えるにつれて、分子の定義も進化してきた。初期の定義では、分子を「その組成と化学的性質を保持する純粋な化学物質の最小の粒子」と定義していたが、あまり正確ではなかった。しかし、岩石、塩類、金属など身近な物質の多くは、化学的に結合した原子やイオンの大きな結晶ネットワークで構成されており、個別の分子でできている訳ではないため、この定義はしばしば破綻する。
現代の分子の概念は、レウキッポスやデモクリトスなど、すべての宇宙は原子と空隙で構成されていると主張した科学以前のギリシャの哲学者までさかのぼることができる。紀元前450年頃、エンペドクレスは、基本元素(火()、土()、空気()、水())と、それらの元素が相互作用する引力と斥力という「力」を想像した。
第5番目の元素である「不壊(ふえ)の真髄」であるエーテルは、天体の基本的な構成要素と考えられていた。レウキッポスやエンペドクレスの視点は、エーテルとともにアリストテレスに受け入れられ、中世およびルネサンス期のヨーロッパに受け継がれた。
しかし、より具体的には、「分子」、すなわち原子が結合した集合体や単位という概念は、ロバート・ボイルが1661年に出版した有名な著書『懐疑的化学者(The Sceptical Chymist)』の中で、「物質は微粒子の集団から構成されており、化学変化はその集団の再編成によって生じる」とした彼の仮説に端を発している。ボイルは、物質の基本要素は「微粒子(corpuscles)」と呼ばれる種類や大きさの異なる粒子で構成されており、これらの粒子は自身を集団に編成することができると主張した。1789年に、ウィリアム・ヒギンズが、原子価結合の概念を予示となる「究極の」粒子の組み合わせと呼ぶものについての見解を発表した。ヒギンズによれば、たとえば酸素の究極粒子と窒素の究極粒子の間の力は6であり、力の強さはそれに応じて分割され、他の究極粒子の組み合わせについても同様である。
ジョン・ドルトンが1803年に原子論を、1804年に倍数比例の法則により原子の存在を提唱した。しかし現代の電子と原子核から構成される粒子のような構造的な概念ではなく、化学反応が一定の単位質量を基に進行するという量的概念であった。
「分子(molecule)」という言葉はアメデオ・アヴォガドロが作り出した。1811年の論文「物体の素分子の相対質量の決定に関するエッセイ」(Essay on Determining the Relative Masses of the Elementary Molecules of Bodies)で、彼は本質的に次のように述べている。すなわち、パーティントンの『化学の歴史(A Short History of Chemistry)』によると、
こうした考え方と同調して、1833年にフランスの化学者マルク・アントワーヌ・オーギュスト・ゴーダンは、アボガドロの原子量に関する仮説を、直線状の水分子のような半正確な分子形状と、H2Oのような正確な分子式の両方を明確に示す体積図(volume diagrams)を使って明確に説明した。
1917年、ライナス・ポーリングという無名のアメリカの化学技術者が、原子間結合を記述する方法として当時主流であったドルトンのフックアンドアイ結合を研究していた。しかし、ポーリングはこの方法に満足せず、新たな分野である量子物理学に新しい方法を求めた。1926年、フランスの物理学者ジャン・ペランが、分子の存在を決定的に証明したことによりノーベル物理学賞を受賞した。彼は、いずれも液相系に関する3種類の方法で計算することによりアボガドロ定数を決定した。1番目はガンボージ石鹸のようなエマルションを使用し、2番目はブラウン運動を実験的に研究し、3番目はアインシュタインの液相における粒子回転の理論を検証した。
1927年、物理学者フリッツ・ロンドンとヴァルター・ハイトラーは、新しい量子力学を、水素分子における可飽和性で非動的な引力と斥力、すなわち交換力の取り扱いに適用した。この問題を原子価結合の観点から扱った彼らの共同論文は、化学を量子力学の下に置くという点で画期的であった。彼らの研究は、博士号を取得したばかりのポーリングに影響を与え、グッゲンハイム・フェローシップでチューリッヒのハイトラーやロンドンを訪問した。
その後、1931年にポーリングは、ハイトラーとロンドンの研究、およびルイスの有名な論文に見られる理論に基づいて、量子力学を用いて分子の性質や結合角・結合に伴う回転といった構造式を計算する画期的な論文「化学結合の本性(The Nature of the Chemical Bond)」を発表した。これらの概念に基づいて、ポーリングは、4つの sp³ 混成軌道が水素の 1s 軌道に重なって4つの σ結合を形成する CH4 のような分子の結合を説明する混成理論を開発した。この4つの結合は同じ長さと強さであるため、下図に示すような分子構造になる。
分子科学
分子科学(molecular science)は、化学と物理のどちらに重点を置くかによって、「分子化学(molecular chemistry)」または「分子物理学(molecular physics)」と呼ばれる。分子化学は、化学結合の形成や切断といった分子間の相互作用を支配する法則を扱い、分子物理学は、分子の構造や特性を支配する法則を扱う。しかし、実際にはこの区別は曖昧である。分子科学では、分子は2つ以上の原子が結合した安定した系(束縛状態)で構成されている。多原子イオンも電気を帯びた分子と見なすことができる。不安定分子(unstable molecule)という用語は、非常に反応性の高い種、すなわちラジカル、分子イオン、リュードベリ分子、遷移状態、ファンデルワールス錯体、ボース=アインシュタイン凝縮のような原子の衝突系など、電子と原子核の一時的な集合体(共鳴)に対して使用される。
分子の形態
物質の構成要素としての分子はありふれたものである。それらはまた、海や大気の大部分を構成している。ほとんどの有機物は分子である。タンパク質とその材料となるアミノ酸、核酸(DNAとRNA)、糖、炭水化物、脂質、ビタミンなど、生命を構成する物質は分子である。栄養素であるミネラルは、一般にイオン化合物であり、分子ではない(例:硫酸鉄)。
しかし、地球上の身近な固体物質の大半は、部分的または全部が結晶やイオン化合物でできており、分子でできているわけではない。これらには、地球の物質を構成するすべての鉱物、砂、粘土、小石、岩、巨礫、地殻、マントル、地球の核などが含まれる。これらはすべて、多くの化学結合を含んでいるが、識別可能な分子でできているわけではない。
塩や共有結合結晶については、グラフェンのように平面的に、あるいはダイヤモンド、石英、塩化ナトリウムのように3次元的に広がる単位格子の繰り返しで構成されていることが多く、典型的な分子を定義することはできない。また、金属結合を伴う凝縮相(固体または液体)であるほとんどの金属にも、単位格子構造の繰り返しという論旨は当てはまる。したがって、固体金属は分子でできているわけではない。ガラスは、ガラス質の無秩序な状態で存在する固体であり、原子は化学結合によって結合しているが明確な分子は存在せず、塩、共有結合結晶、金属を特徴づける単位格子構造を繰り返す規則性も存在しない。
結合
一般に、分子は共有結合によって結ばれている。いくつかの非金属元素は、自由原子としては存在せず、環境中では化合物または等核分子としてのみ存在するものがある。水素はその例である。
金属結晶は、金属結合によってまとめられた1つの巨大な分子と見なすことができると言う人もいれば、金属は分子とはまったく異なるふるまいをすると指摘する人もいる。
共有結合
共有結合(covalent bond)は、原子と原子の間で電子対(電子の組)を共有する化学結合である。これらの電子対を「共有対」または「結合対」と呼び、原子間で電子を共有するときの引力と斥力(反発力)が安定した均衡をもたらす状態を「共有結合」と呼ぶ。
イオン結合
イオン結合(ionic bonding)は、逆荷電を持つイオン間で静電引力を伴う化学結合の一種で、イオン化合物で生じる主要な相互作用である。イオンとは、1つまたは複数の電子を失った原子(カチオン)と、1つまたは複数の電子を獲得した原子(アニオン)のことである。このような電子の移動は、共有結合とは対照的に「電気原子価(electrovalence)」と呼ばれる。最も単純なケースでは、カチオンは金属原子、アニオンは非金属原子であるが、イオンの中にはNH4+やSO42−のような分子イオンのように、より複雑な性質を持つものも存在する。常温常圧では、ほとんどの場合、イオン結合は個別に識別可能な分子を持たない固体(場合によっては液体)を形成するが、そのような物質が気化/昇華すると個別の分子が生じる(結合が(共有結合ではなく)イオン結合と見なされるだけの十分な電子が移動する)。
分子の大きさ
ほとんどの分子は肉眼で見ることができないほど小さいが、DNAのような生体高分子を含む多くのポリマーの分子は巨視的な大きさに達することがある。有機合成の構成要素として用いられる分子の大きさは、一般的に数オングストローム(Å)から数十オングストローム(10億分の1メートル)程度である。この大きさでは可視光の波長以下の為、顕微鏡など光学的な像として個々の分子を観察することはできない。したがって通常目にする物質は結晶やクラスターなど集団としての分子を目にしていることになる。分子の単位質量は分子量が用いられ、およそ分子量で103から104を境に、それ以下の分子を低分子、それ以上の分子を高分子と呼ぶ。
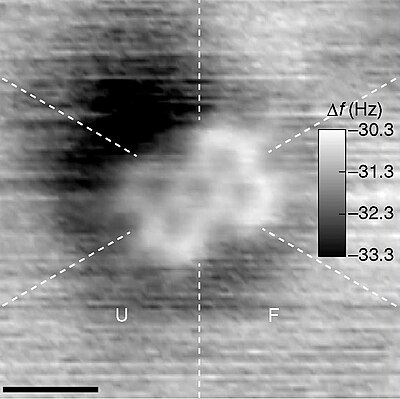
単一の分子の姿は測定器を介して観測するしかないが、原子間力顕微鏡(AFM)を用いると、低分子(小分子)や個々の原子の輪郭を追跡できることがある。もっとも大きな分子には超分子がある。最も小さな分子は二原子水素(H2)で、結合長は0.74 Åである。
有効分子半径は、溶液中で分子が示す大きさである。各物質の透過選択性の表にその例が示されている。
分子式
化学式の種類
分子の化学式は、元素記号や数字のほか、丸かっこ、ダッシュ(')、角かっこ([])、プラス(+)、マイナス(-)などの記号を用いて1行で表示する。これらは下付き文字と上付き文字を含むこともあり、活版印刷の1行で表現できるように制限されている。
化合物の実験式は、非常に単純な種類の化学式である。これは、化合物を構成する化学元素の最も単純な整数比のことである。たとえば、水は常に水素原子と酸素原子が2:1の比率で構成され、エタノール(エチルアルコール)は常に炭素、水素、酸素が2:6:1の比率で構成されている。ただし、これによって分子の種類を一意に決めるものではなく、たとえばジメチルエーテルはエタノールと同じ比率である。同じ原子を異なる配置で持つ分子を異性体と呼ぶ。また、たとえば炭水化物は同じ比率(炭素:水素:酸素=1:2:1。したがって実験式も同じ)を持つが、分子内の総原子数は異なる。
分子式は、分子を構成する原子の正確な数を反映し、異なる分子を特徴づける。ただし、異なる異性体は、異なる分子であっても、同じ原子組成を持つことがある。
実験式と分子式が同じであることがよくあるが、常にそうとは限らない。たとえば、アセチレン分子の分子式はC2H2であるが、その元素の最も単純な整数比はCHである。
分子量は、化学式から計算することができ、中性炭素12(12C同位体)原子の質量の1/12に相当する通常の原子質量単位で表される。ネットワーク固体の場合、化学量論的計算の際に式単位という用語を使用する。
構造式
複雑な3次元構造を持つ分子、特に4つの異なる置換基と結合した原子を含む分子では、単純な分子式や示性式でさえ、分子を完全に特定できない場合がある。そのような場合には、構造式と呼ばれるグラフィカルな式が必要になることがある。構造式は一次元の化学名で表すこともできるが、そうした化学命名法には化学式の一部に含まれない多くの単語や用語が必要である。
分子構造
分子は、平衡幾何構造(結合の長さや角度)が決まっており、振動や回転によって連続的に運動している。純物質は、同じ平均的な幾何構造を持つ分子で構成されている。分子の化学式と構造は、その分子の性質、特に反応性を決定する重要な要素である。異性体は、化学式は同じだが構造が異なるため、通常、性質が大きく異なる。立体異性体という特種な異性体は、非常によく似た物理化学的性質を持つと同時に、異なる生化学的活性を持つことがある。
分子分光法
分子分光法(ぶんしぶんこうほう、英: molecular spectroscopy)は、エネルギー(プランクの公式による周波数)が既知のプローブ信号に相互作用する分子の応答(スペクトル)を扱う分析手法である。分子はエネルギー準位が量子化されており、分子のエネルギー交換を吸光または発光で検出することで分析することができる。一般に分子分光法は、中性子・電子・高エネルギーX線などの粒子が(結晶のように)規則的に配置された分子と相互作用する回折研究を指すものではない。
マイクロ波分光法は、分子の回転の変化を測定し、宇宙空間にある分子を識別するために一般に利用される。赤外線分光法は、分子の伸縮、屈曲、ねじれなどの振動を測定する。これは、分子内の結合や官能基の種類を特定するために一般に使用される。電子の配列の変化により、紫外光、可視光、または近赤外光に吸収線や輝線が生じ、色が発生する。核磁気共鳴分光法は、分子内の特定の原子核の環境を測定し、分子内の異なる位置にある原子の数を特徴付けるために使用される。
理論的側面
分子物理学や理論化学による分子の研究は、主に量子力学に基づいており、化学結合を理解するうえで不可欠である。最も単純な分子は水素分子イオン H2+であり、すべての化学結合の中で最も単純なものは1電子結合である。H2+は正荷電の陽子2個と負荷電の電子1個で構成され、電子間反発がないため、この系のシュレーディンガー方程式はより簡単に解くことができる。高速デジタルコンピューターの発達により、より複雑な分子に対する近似解が可能になり、計算化学の主要な一面を担っている。
IUPACは、ある原子配列が分子として「十分に安定か」どうかを厳密に定義しようとする場合、「少なくとも1つの振動状態を閉じ込めるのに十分な深さのポテンシャルエネルギー曲面上のくぼみに対応する必要がある」と提案している。この定義は、原子間の相互作用の性質には依存せず、相互作用の強さのみに依存する。実際、ヘリウムの二量体であるHe2は、振動結合状態が1つで、結合が非常に弱いため、極低温でしか観測されない可能性があるが、こうした弱い結合の種も分子と見なされている。
原子の配列が「十分に安定か」どうかは、本質的には運用上の定義である。したがって、哲学的には分子は基本的な実体ではなく(たとえば素粒子と対照的)、むしろ分子という概念は、化学者が、私たちが観察する世界における原子スケールでの相互作用の強さについて、有用な意見を述べる方法である。
出典
参考文献
- 『現代化学史 原子・分子の化学の発展』Noboru Hirota, 襄 廣田、京都大学学術出版会、2013年10月5日、45頁。ISBN 978-4-87698-283-7。OCLC 862767435。https://www.worldcat.org/oclc/862767435。
関連項目
外部リンク
- 『分子』 - コトバンク
- 今月の分子 (Molecule of the Month) - ブリストル大学, 化学科 (英語)
Text submitted to CC-BY-SA license. Source: 分子 by Wikipedia (Historical)
Owlapps.net - since 2012 - Les chouettes applications du hibou